新型肺炎最新研究成果发布,抗病毒药物初步测试

李兰娟院士(第一排中间)与武汉大学人民医院医生交流新的治疗方案。 记者黄琪 摄
2020年2月4日,中国工程院院士、国家卫健委高级别专家组成员李兰娟团队,在武汉公布治疗新型冠状病毒感染的肺炎的最新研究成果。
李兰娟院士说,根据初步测试,在体外细胞实验中显示:(1)阿比朵尔在10~30微摩尔浓度下,与药物未处理的对照组比较,能有效抑制冠状病毒达到60倍,并且显著抑制病毒对细胞的病变效应。(2)达芦那韦在300微摩尔浓度下,能显著抑制病毒复制,与未用药物处理组比较,抑制效率达280倍。
李兰娟院士说,抗艾滋病药物克力芝对治疗新型冠状病毒感染的肺炎效果不佳,且有毒副作用。她建议将以上两种药物列入国家卫健委《新型冠状病毒感染的肺炎诊疗方案(试行第六版)》。
李兰娟院士团队成员、浙江援鄂重症救治组领队、浙大一院副院长陈作兵提醒,“这两种药为处方药,患者一定要在医生的指导下服用。”他还介绍,现在这两种药物已经在浙江省新型冠状病毒感染的肺炎患者中使用,下一步计划用这两种药物替代其他效果欠佳的药物。(来源:长江日报,记者黄琪)
科普知识:新型冠状病毒的基本生物学特性,新冠肺炎患者早期病毒核酸量更高
中国科学院武汉病毒所研究员石正丽说:“2019新型冠状病毒是大自然给人类不文明生活习惯的惩罚,和实验室没有关系。”
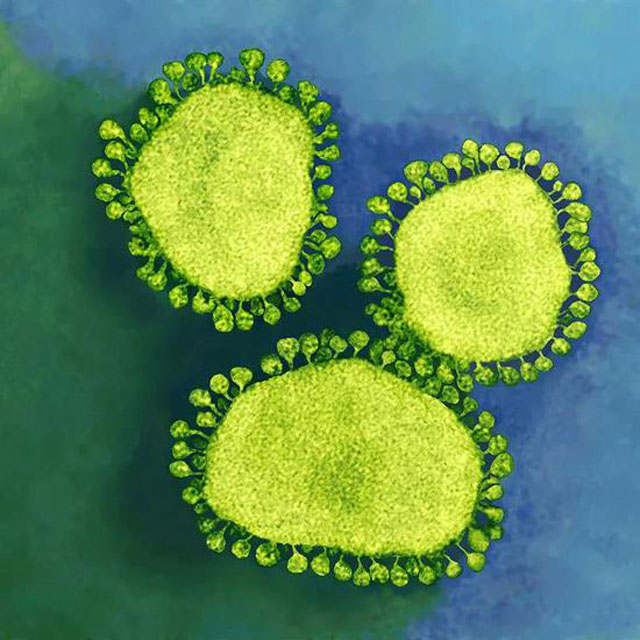
(Credit: Dr Linda Stannard/UCT/Science Photo Library)
1月23日,中国科学院武汉病毒研究所石正丽团队针对引起武汉肺炎疫情的新型冠状病毒的鉴定工作在论文预印网站公布。2月3日,Nature杂志正式发表了这一研究,论文标题标题为“Pneumonia outbreak is associated with a novel coronavirus of likely bat origin”。中科院武汉病毒所周鹏研究员、杨兴娄副研究员和金银谭医院的王先广医生为该论文共同第一作者,武汉病毒所石正丽研究员为通讯作者。
文章从核酸检测、血清学诊断、病毒分离和受体利用等方面揭示出该冠状病毒的基本生物学特性,为疫情控制和药物研发等工作提供了重要线索。
研究团队从早期的5位患者样本中获得了该病毒的全基因组序列,来自5位患者的病毒序列相似性达到99.9%,与SARS-CoV的序列一致性为79.5%。通过对病毒保守蛋白氨基酸分析发现2019-nCoV与SARS病毒属于同一种冠状病毒(SARS-related coronavirus, SARSr-CoV)。
作者进一步将2019-nCoV基因组与实验室早期检测的冠状病毒的部分基因序列进行比较,发现该病毒与来源于蝙蝠样本的一株冠状病毒(简称TG13)的基因相似,后对该蝙蝠样本进行测序,获得了蝙蝠病毒TG13的全基因组序列,发现两种病毒序列一致性高达96%。
值得注意的是,科研团队对患者不同时期的支气管肺泡灌洗液、咽拭子、肛拭子等样本进行了两轮核酸检测,时间分别为2019年12月30日和2020年1月10日,结果发现前一个时间样本的病毒核酸量比后期高约1000倍以上。采用实验室早期储备的SARSr-CoV抗原,对患者血清样本进行了检测,发现患者产生了相应的IgM和IgG抗体。随后从一位重症患者的支气管肺泡灌洗液中,分离获得了2019-nCoV病毒,电镜观察可见其在细胞内清晰的冠状病毒颗粒形态。
研究团队发现,2019-nCoV能感染过表达人ACE2(血管紧张素转换酶,SARS-CoV的细胞受体非敏感细胞,表明2019-nCoV可以利用SARS-CoV的相同受体入侵细胞。研究还表明2019-nCoV可以利用SARS-CoV的受体感染细胞,为后续疫情防控和药物研究等奠定了重要工作基础。
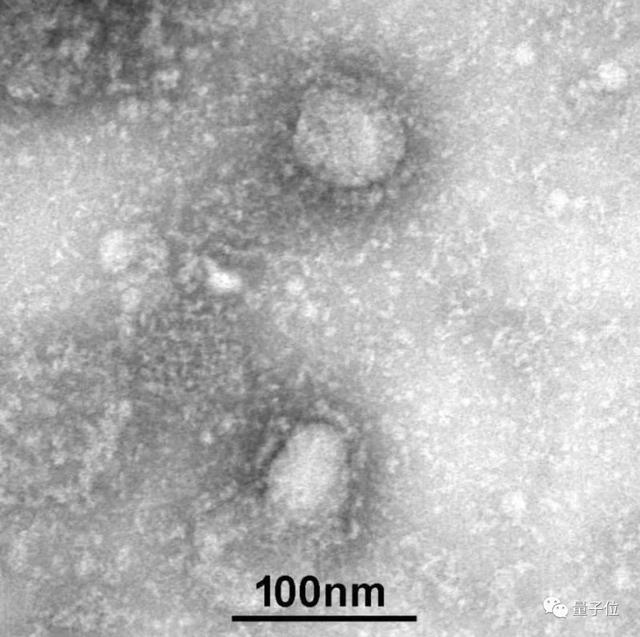
图:1月24日,中国疾控中心成功分离首株新型冠状病毒毒种。
1月11日,复旦大学张永振教授团队在virologic.org网站发布首个新型冠状病毒基因序列。第二天,国家卫健委领导的小组在全球共享流感病毒数据库GISAID发布了另外5个来自不同患者的病毒基因组序列。
1月24日,中国疾控中心成功分离首株新型冠状病毒毒种。其信息及电镜照片、新型冠状病毒核酸检测引物和探针序列等均由国家病原微生物库权威发布,并提供共享服务。
中国科研人员的迅速行动,为全球科学家研究新型冠状病毒提供了坚实基础,许多研究机构都得以立即展开疫苗药物等研究。
早在2015年《自然医学》发表的论文中,由美国北卡罗莱纳大学教堂山分校主导的一项研究结果,研究人员们使用SARS-CoV反向遗传系统,生成并鉴定了一种类SARS新型冠状嵌合病毒。石正丽是论文作者之一。
体内实验证明,嵌合病毒在小鼠肺中的复制具有明显的发病机理,能感染小鼠呼吸道细胞而引发严重急性呼吸系统综合征。这项工作表明,蝙蝠种群中流行的病毒,可能会再次重现类似SARS的传播风险。
据Nature报道,这项研究当时确实引发了风险辩论,比如,巴黎巴斯德研究所的病毒学家Simon Wain-Hobson就认为:“如果病毒逃脱,那么谁也无法预测后果。”
也有信息生物学学者撰文进一步解释,为什么这四个原始序列重合并不能有任何价值。认为:新型冠病毒与HIV的序列匹配非常短,出现在两种病毒的高变区中,在2019-nCoV序列与许多其他生物之间也发现了相似的重叠。从理论上讲,HIV序列可以赋予另一种病毒的独特生物学特性在2019-nCoV中完全缺失,并且2019-nCoV没有已知的冠状病毒可能无法实现的独特临床特性。
新冠病毒的临床表现也不具有需要解释的新颖特征。它的症状特征,可传播程度,严重性,死亡率,持续时间,潜伏期和潜伏期,从动物传播到人类的能力以及无症状和皮肤接触的传播能力,均在其他人类冠状病毒中成立。到目前为止,没有证据表明2019-nCoV可以感染T细胞,或者可以感染任何表达CD4的细胞,或者可以感染任何不表达ACE2或不能被其他已知冠状病毒感染的细胞。(来源:中国科学院网,《自然》杂志,新浪科技-量子位)
推荐
-

-

QQ空间
-

新浪微博
-

人人网
-

豆瓣






